Soutenance de Thèse : Shijia Wu
| Quand ? |
Le 19/09/2025, de 14:00 à 17:00 |
|---|---|
| Où ? | Salle des thèses |
| S'adresser à | Shijia Wu |
| Participants |
Marie-Stephanie CLERGET-FROIDEVAUX, Professeure Museum National d'Histoire Naturelle de Paris, rapporteure; Beatriz MORTE, Chercheuse, CIBERER, rapporteure; Gérard BENOIT, Chargé de recherche - HDR, Université de Rennes / CNRS, Examinateur; Marie SEMON, Professeur ENS de Lyon, Examinateur; Frédéric FLAMANT, Directeur de recherche, ENS de Lyon / INRAE, Directeur de these; Wenzheng JIANG Professeur, ECNU; Co-directeur de these. |
| Ajouter un événement au calendrier |
|
Le 19 septembre, Shijia Wu de l'équipe de Frédéric Flamant soutiendra sa thèse intitulée :
"Identification of Thyroid Hormone Receptors Target Genes: In Vitro Analysis and In Vivo Exploration in Mouse Hypothalamus"

Résumé :
Les hormones thyroïdiennes (HT, dont la thyroxine et la 3,3’,5-triiodo-L-thyronine, ou T3, son métabolite actif) sont essentielles tout au long de la vie. Elles régulent les processus de développement et maintiennent l’homéostasie systémique à l’âge adulte, exerçant leur action en se liant à des récepteurs nucléaires (TR, dont TRα1 et TRβ1), présents dans pratiquement tous les types cellulaires. Les TR forment des hétérodimères avec les récepteurs des rétinoïdes X (RXR) et se lient à l’ADN sur des éléments de réponse largement répandus dans le génome. La liaison des HT induit le remodelage de la chromatine et active la transcription des gènes voisins.
L’objectif principal de la thèse était de comprendre la fonction des HT dans l’hypothalamus de la souris adulte, une zone cérébrale qui joue un rôle central dans la régulation de l’équilibre énergétique. L’hypothalamus intègre des signaux hormonaux et neuronaux pour contrôler la température, l’appétit, les rythmes circadiens et la dépense énergétique, autant de fonctions physiologiques sensibles aux HT. Il régule également le taux circulants d’HT, via l'axe hypothalamo-hypophyso-thyroïdien (HPT).
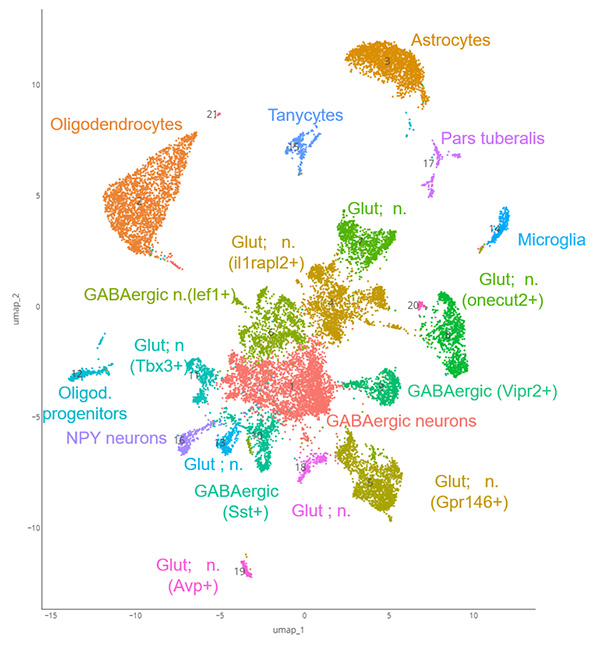
Pour identifier les gènes cibles des TR dans les types cellulaires de l'hypothalamus, nous nous sommes concentrés sur deux critères : la présence de sites de liaison des TR dans les séquences régulatrices des gènes et l'expression des gènes sensibles à T3. Nous nous sommes appuyés sur un atlas des sites de liaison des TR identifiés dans divers tissus et types cellulaires, dont une fraction est commune à tous les types cellulaires. La première partie de la thèse décrit une analyse in vitro de ces éléments de réponse putatifs aux TR. Nous avons développé la méthode SOSHI-seq (Screening of self-transcribed hormone-inducible elements sequencing), un test rapporteur in vitro à haut débit qui consiste à placer des fragments d'ADN dans la partie transcrite d'un vecteur plasmidique. L'activité d'un fragment d'ADN lui permet de renforcer sa propre transcription de manière dépendante de T3. Le SOSHI-seq est donc une procédure générale permettant de tester la présence d'éléments fonctionnels sensibles à T3 dans des fragments d'ADN génomique. En criblant 2 000 fragments, nous avons identifié environ 500 éléments activés par T3, dont beaucoup contenaient des motifs DR4 canoniques (AGGTCANNNNAGGTCA). Les dosages de la luciférase ont confirmé et précisé les résultats du SOSHI-seq. Pour profiler les gènes in vivo, nous avons traité des souris avec du propylthiouracile afin de réduire le niveau de THs. Nous avons ensuite traité les souris avec de la TH et réalisé un séquençage d'ARN nucléaire (SnRNA-seq) sur l'hypothalamus médiobasal des souris, combiné à un séquençage par RNA-seq de différents types cellulaires triés. Nous avons identifié la réponse à T3 de 21 groupes cellulaires. Afin d'examiner les rôles physiologiques de la signalisation T3 dans l’hypothalamus, nous avons généré deux lignées de souris exprimant un TRα1 dominant-négatif afin de bloquer la signalisation T3 dans les astrocytes ou les oligodendrocytes. L’expression innattendue de la mutation dans le pancréas, a cependant empêché d’interprétation ces données. En résumé, notre étude fournit une analyse multidimensionnelle de la signalisation des HT dans l'hypothalamus. Ces résultats apportent un nouvel éclairage sur les actions spécifiques des cellules T3 dans le cerveau et soulignent le rôle de l'hypothalamus dans la régulation du métabolisme.